Az oldal tölt...
248
248
| Kategória: |
Definíció
|
Évfolyam: |
9. |
| Kulcsszó: |
Fázisdiagram |
Lektorálás: |
Nem lektorált |
Fázisdiagram
Egy anyag fázisdiagramja az adott anyag halmazállapotait ábrázolja egy p-T diagramon.
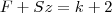
, ahol
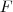
a fázisok száma,
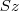
a szabadsági fokoké,
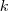
pedig a kémiailag tiszta, egynemű anyagoké.
Az egyenlet megértését segítheti a következő példa: a víz esetén a kémiailag tiszta, egynemű anyaghalmazok száma egy, a víz. A gőznyomás görbén(cseppfolyós-gőz) megváltoztathatjuk a nyomást vagy a hőmérsékletet, mivel a másik állapotjelző egyidejű változtatásával fenntarthatjuk a két fázist, de egymástól függetlenül nem változtathatjuk őket, ezért a szabadsági fokok száma 1. Mivel két fázis van, így az egyenlet teljesül(1+2=3).
A legnagyobb hőmérséklet, ami esetén egy anyag még cseppfolyós lehet, a kritikus hőmérséklet. Ez alatt a légnemű fázist gőznek, e fölött gáznak nevezzük.
Az ábra a Horváth Miklós által készített lexikon része(http://www.freeweb.hu/hmika/Vilag.htm).
A három görbe a hármasponton találkozik, ahol egyszerre van jelen a szilárd, a cseppfolyós és a gőz fázis.
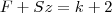 , ahol
, ahol 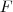 a fázisok száma,
a fázisok száma, 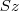 a szabadsági fokoké,
a szabadsági fokoké, 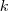 pedig a kémiailag tiszta, egynemű anyagoké.
pedig a kémiailag tiszta, egynemű anyagoké.




